更多“在电池反应中,当反应物与产物达到平衡时,该电池反应的电势等于…”相关的问题
更多“在电池反应中,当反应物与产物达到平衡时,该电池反应的电势等于…”相关的问题
| 广泛,摩托罗拉公司也开发出一种由甲醇、氧气以及强碱做电解质溶液的新型手机电池,容量达氢镍电池或锂电池的10倍,可连续使用一个月才充一次电。请完成下列与甲醇有关的问题。 工业上有一种生产甲醇的反应为: |
 |
| 在温度和容积相同的A、B两个容器中,按不同方式投人反应物,保持恒温恒容,经10秒钟后达到平衡,达到平衡时的有关数据如下表 |
|
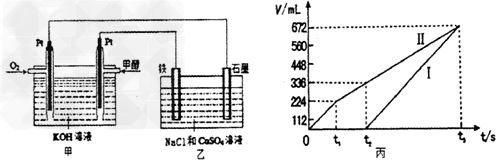
| (1)从反应开始到达到平衡时,A中用CO2来表示的平均反应速率为_________。 (2)A中达到平衡时CO2的转化率为_________。 (3)a =_________。 某同学设计了一个甲醇燃料电池,并用该电池电解200mL一定浓度NaCl与CuSO4混合溶液,其装置如图 |
|
| (4)写出甲中通入甲醇这一极的电极反应式__________________ (5)理论上乙中两极所得气体的体积随时间变化的关系如丙图所示(气体体积已换算成标准状况下的体积),写出在t1后,石墨电极上的电极反应式__________________;在t2时所得溶液的pH为__________________。(假设溶液体积不变) |
A.两电对BrO3-/Br-与I2/2I-的电位相等
B.反应产物I2与KBr的物质的量相等
C.溶液中已无BrO3-离子存在
D.反应中消耗的KBrO3的物质的量与产物I2的物质的量之比为1:3
A、大于35%
B、等于35%
C、小于35%
D、无法知道
已知反应NiO(s)+CO(g)=Ni(s)+CO2(g)的
Kθ(936K)=4.54×102.Kθ(1027K)=2.55×103.若在上述温度范围内△Cp=0p(1)试求此反应在1000K时的△rGmθ、△rHmθ原和△rAmθ;(2)若产物中的镍与某金属生成固溶体(合金),当反应在1000K达到平衡
时,p(CO2)/p(CO)-1.05×103求固溶体中镍的活度,并指出所选的标准态.
298K时,在Ag+/Ag电极中加入过量I-,设达到平衡时c(I-)=0.1mol·dm-3,而另一电极为Cu2+/Cu,c(Cu2+)=0.01mol·dm-3,将两电极组成原电池,写出原电池符号、电池反应,并求电池反应平衡常数。
已知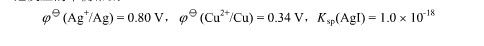
可使任何反应达到平衡时增加产率的措施是()。
A.升温
B.加压
C.增加反应物浓度
D.加催化剂
可逆反应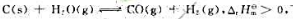 下列说法正确的是().
下列说法正确的是().
A、达到平衡时反应物和生成物的分压相等
B、降低温度有利平衡向正反应方向移动
C、升高温度有利于平衡向正反应方向移动
D、增大压力对平衡没有影响
A.达到平衡时,反应物的浓度和生成物的浓度相等
B.达到平衡时,反应物和生成物的浓度不随时间的变化而变化
C.由于反应前后分子数相等,所以增加压力对平衡没有影响
D.升高温度使正反应速率增大,逆反应速率减小,结果平衡向右移


 如果结果不匹配,请
如果结果不匹配,请