 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[单选题]
已知反应A 2B的速率方程为r=kcA,则该反应的半衰期t1/2为()
A.2ln2/k;
B.ln2/2k;
C.4ln2/k;
D.ln2/k;
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.2ln2/k;
B.ln2/2k;
C.4ln2/k;
D.ln2/k;
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知反应A 2B的速率方程为r=kcA,则该反应的半衰期t1…”相关的问题
更多“已知反应A 2B的速率方程为r=kcA,则该反应的半衰期t1…”相关的问题
行时,其半衰期为6.93min,且知在两个pH值的各自条件下,t1/2均与A的初始浓度无关,设反应的速率方程为


(A) 125kJ·mol-1(B) 519kJ·mol-1(C) 53.9 kJ·mol-1(D) 62kJ·mol-1
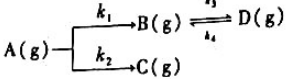
反应开始时只有A(g),且已知CA.o=2.0mol·dm-3,k=3.0s-1,kz=2.5s-1,k3=4.0s-1,k4=5.0s-1.
(1)试写出分别用cA,CB,Cc,CD表示的速率方程;
(2)求反应物A的半衰期;
(3)当反应物A完全反应(即cA=0)时,CB,Cc,CD各为多少?
反应2A+B→A2B是一基元反应,某温度时,当两反应物的浓度均为0.01mol·dm-3时,初始反应速率为2.5×10-3mol·dm-3·s-1。当A的浓度为0.015mol·dm-3,B的浓度为0.030mol·dm-3时,初始反应的速率是多少?
高温时NO2分解为NO和O2,其反应速率方程为
-v(NO2)=kc2(NO2)
在592K时,速率常数是4.98×10-1L·mol-1·s-1;在656K时,其值变为 4.74L·mol-1·s-1,计算该反应的活化能。