 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知在Ca3(PO4)2的饱和溶液中,c(Ca2+)=2.0×10-6mol.L-1,C(PO43-)=1.58×10-6mol.L-1,则Ca3(PO4)2
已知在Ca3(PO4)2的饱和溶液中,c(Ca2+)=2.0×10-6mol.L-1,C(PO43-)=1.58×10-6mol.L-1,则Ca3(PO4)2的Ksp为()。
A.2.0×10-29
B.3.2×10-12
C.6.3×10-18
D.5.1×10-27
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案


 更多“已知在Ca3(PO4)2的饱和溶液中,c(Ca2+)=2.0…”相关的问题
更多“已知在Ca3(PO4)2的饱和溶液中,c(Ca2+)=2.0…”相关的问题
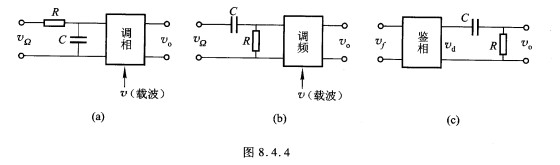 1)在图(a)中,设vΩ(t)=VΩcos(2π×103t),v=V0cos(2π×106t)。已知R=30 kΩ,C=0.1μF或R=10 kΩ,C=0.01μF。 2)在图(b)中,设vΩ(t)=VΩcos(2π×103t),v=V0cos(2π×106t)。已知R=10 kΩ,C=0.01μF或R=100 Ω,C=0.03 μF。 3)在图(c)中,设Vf(t)=Vfcos(ω0t+mfsinΩt)。已知R=100 Ω,C=0.03 μF。鉴相特性为Ap△θ。
1)在图(a)中,设vΩ(t)=VΩcos(2π×103t),v=V0cos(2π×106t)。已知R=30 kΩ,C=0.1μF或R=10 kΩ,C=0.01μF。 2)在图(b)中,设vΩ(t)=VΩcos(2π×103t),v=V0cos(2π×106t)。已知R=10 kΩ,C=0.01μF或R=100 Ω,C=0.03 μF。 3)在图(c)中,设Vf(t)=Vfcos(ω0t+mfsinΩt)。已知R=100 Ω,C=0.03 μF。鉴相特性为Ap△θ。















