 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
电池:Mg2+离子选择电极|Mg2+(6.87×10-3mol/L)‖SCE,其电动势为0.367V。用一未知Mg2+溶液代替上述已知Mg2+溶液
电池:Mg2+离子选择电极|Mg2+(6.87×10-3mol/L)‖SCE,其电动势为0.367V。用一未知Mg2+溶液代替上述已知Mg2+溶液,测得电动势为0.446V,该电极的实际斜率为0.0296V,试计算未知溶液的pMg值。
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
电池:Mg2+离子选择电极|Mg2+(6.87×10-3mol/L)‖SCE,其电动势为0.367V。用一未知Mg2+溶液代替上述已知Mg2+溶液,测得电动势为0.446V,该电极的实际斜率为0.0296V,试计算未知溶液的pMg值。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“电池:Mg2+离子选择电极|Mg2+(6.87×10-3mo…”相关的问题
更多“电池:Mg2+离子选择电极|Mg2+(6.87×10-3mo…”相关的问题
A、4.0
B、4.5
C、5.5
D、5.0
0.4000g牙膏样品加50.0ml含有柠檬酸盐缓冲剂和NaCl的溶液共沸以分离F-,冷却后溶液稀释到100ml。取25.00ml,以氟离子选择电极/饱和甘汞电极系统测量,电动势为-0.182V,加入0.00107mg/ml的F-标准溶液5.00ml,测得电动势为-0.145V。计算样品中F-的含量(mg/g)。
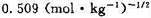 。试求:(1)电极反应和电池反应;(2)电池的标准电动势
。试求:(1)电极反应和电池反应;(2)电池的标准电动势 (要考虑γ±的影响);(3)按电池反应有2个电子得失,当反应进度为1mol时的
(要考虑γ±的影响);(3)按电池反应有2个电子得失,当反应进度为1mol时的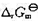 .
.