 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
试用价层电子对互斥理论判断下列分子或离子的空间构型,并指出其中心原子的杂化方式。
试用价层电子对互斥理论判断下列分子或离子的空间构型,并指出其中心原子的杂化方式。
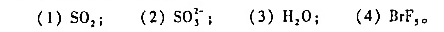
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
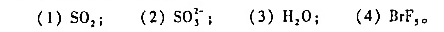
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“ 试用价层电子对互斥理论判断下列分子或离子的空间构型,并指出…”相关的问题
更多“ 试用价层电子对互斥理论判断下列分子或离子的空间构型,并指出…”相关的问题
A.正四面体,sp3杂化
B.三角锥形,不等性sp3杂化
C.正方形,dsp2杂化
D.正三角形,sp2杂化
(1)HgCl2(直线形);(2)SiF4(正四面体);(3)BCl3(平面三角形);
(4)NF3(三角锥形,102°);(5)NO2-(V形,115.4°);(6)SiF62-(八面体).