更多“已知汞溶胶中粒子(设为球形)的直径为22nm,在1.0dm3…”相关的问题
更多“已知汞溶胶中粒子(设为球形)的直径为22nm,在1.0dm3…”相关的问题
第1题
下列关于溶胶剂的错误表述是()。
A.溶胶剂属于热力学和动力学均不稳定体系
B.溶胶剂中加入电解质会产生盐析作用
C.溶胶粒子具有双电层结构而荷电,溶胶具有电泳现象
D.ξ电位越高斥力越大,溶胶剂的稳定性越差
E.溶胶粒子越小,布朗运动越激烈,因而沉降速度越小
第2题
下列关于溶胶剂的正确表述是()。A.溶胶剂属于热力学稳定体系B.溶胶剂中加入电解质会产生盐析作用
下列关于溶胶剂的正确表述是()。
点击查看答案
A.溶胶剂属于热力学稳定体系
B.溶胶剂中加入电解质会产生盐析作用
C.溶胶粒子具有双电层结构
D.ξ电位越大,溶胶剂的稳定性越差
E.溶胶粒子越大,布朗运动越激烈,因而沉降速度越小
第4题
试根据汞的元素电势图回答问题:①在酸性介质中Hg22+能否发生歧化反应?②计算反应的平
试根据汞的元素电势图回答问题:
点击查看答案
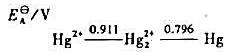
①在酸性介质中Hg22+能否发生歧化反应?
②计算反应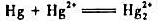 的平衡常数Kθ;
的平衡常数Kθ;
③拟使Hg(I)歧化为Hg(II)和Hg,应该怎样做?试举两个实例加以说明。
第5题
由直径为3mm的多孔球形催化剂组成的等温固定床,在其中进行1级不可逆反应,基于催化剂颗粒体积计算的反应速率
常数为0.8s-1,有效扩散系数为0.013cm2/s。当床层高度为2m时,可达到所要求的转化率。为了减小床层的压力降,改用直径为6mm的球形催化剂,其他条件均不变,流体在床层中流动均为层流。试计算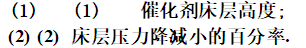
第6题
空胶囊的制备工艺流程为()A.溶胶→干燥→蘸胶—拔壳→切割→整理B.溶胶→蘸胶→干燥—拔壳→切割→整理C.溶
空胶囊的制备工艺流程为()
点击查看答案
A.溶胶→干燥→蘸胶—拔壳→切割→整理
B.溶胶→蘸胶→干燥—拔壳→切割→整理
C.溶胶→蘸胶→拔壳→干燥—整理
D.溶胶→切割→蘸胶→拔壳→干燥→整理
E.溶胶—切割→干燥→蘸胶→拔壳—整理
第8题
下列叙述那些是正确的
A.溶胶剂是澄明的,因此它属于均相分散体系,热力学稳定。
B. 溶胶剂中粒子具有双电层结构,其吸附层离子与反离子形成的电位差称为ζ电位。由于ζ电位的存在整个分散系是带电的。
C. 高分子溶液的稳定性主要是因为水化膜的存在。
D. 在混悬剂中加入电解质使ζ电位降低,混悬粒子形成疏松聚集体,因而降低了混悬剂的稳定性。
第9题
在三支各盛有20mlFe(OH)3溶胶的试管中,分别加入4.2m1, 0.5mol.L-1NaCl溶液,12.5ml,
在三支各盛有20mlFe(OH)3溶胶的试管中,分别加入4.2m1, 0.5mol.L-1NaCl溶液,12.5ml, 0.005mol*L-1Na3SO4溶液,7.5ml, 0.0003mol*L-1Na3PO4溶液,溶胶开始发生凝结,计算各电解质的聚沉值。制备上述Fe(OH)3溶胶时,用稍过量的FeCl3与H2O作用制成的,写出其胶团结构式,指明胶粒的电泳方向。”
点击查看答案



 如果结果不匹配,请
如果结果不匹配,请