 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
工业上对反应2SO?+O?=2SO?+Q使用催化剂的目的是____。
A.扩大反应物的接触面
B.促使平衡向正反应方向移动
C.缩短达到平衡所需的时间,提高SO 的转化率
D.增大产品的产量
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.扩大反应物的接触面
B.促使平衡向正反应方向移动
C.缩短达到平衡所需的时间,提高SO 的转化率
D.增大产品的产量
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“工业上对反应2SO?+O?=2SO?+Q使用催化剂的目的是_…”相关的问题
更多“工业上对反应2SO?+O?=2SO?+Q使用催化剂的目的是_…”相关的问题
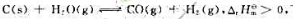 下列说法正确的是().
下列说法正确的是().A、达到平衡时反应物和生成物的分压相等
B、降低温度有利平衡向正反应方向移动
C、升高温度有利于平衡向正反应方向移动
D、增大压力对平衡没有影响
A.加入催化剂只加速了正反应的反应速率
B.某个催化剂对所有反应速率都具有加速作用
C.加入催化剂,正反应速率增大10倍,逆反应速率也增大10倍
D.加入催化剂,不但能加快到达平衡的时间,也能提高转化效率
A.达到平衡时,反应物的浓度和生成物的浓度相等
B.达到平衡时,反应物和生成物的浓度不随时间的变化而变化
C.由于反应前后分子数相等,所以增加压力对平衡没有影响
D.升高温度使正反应速率增大,逆反应速率减小,结果平衡向右移
A.催化剂只能缩短达到平衡的时间而不能改变平衡状态
B.催化剂对反应的加速作用具有选择性
C.催化剂可以改变化学平衡常数
D.催化剂加入不能实现热力学上不可能进行的反应
A.通入氦气使密闭容器中压强增大,平衡向正反应方向移动
B.增加X的物质的量,混合气体的密度减小
C.降低温度,混合气体的平均相对分子质量增大
D.X的正反应速率是Y的逆反应速率的m/n倍
A.因为反应放热,所以升高温度会使反应速率减慢
B.通过调控反应条件,SO 2 可以100%地转化为SO 3
C.当SO 2 与SO 3 的浓度相等时,反应达到平衡
D.使用催化剂的目的是加快反应速率,提高生产效率
B.通入稀有气体使压强增大,平衡将逆向移动
C.若平衡时A.B的转化率相等,说明反应开始时A.B的物质的量之比为 n : m
D.升高温度,混合气体的平均相对分子质量变大
A.具有高度的催化专一性
B.能加快反应速度
C.能缩短反应达到平衡所需的时间
D.反应前后质和量无改变
E.对正,逆反应都有催化作用