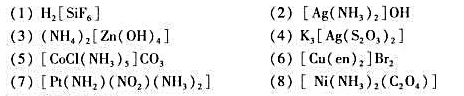更多“在胆矾晶体中,中心离子铜的配位数是:()。”相关的问题
更多“在胆矾晶体中,中心离子铜的配位数是:()。”相关的问题
第4题
离子键定义
下列说法正确的是()
A.金属和非金属元素原子之间形成的化学键不一定是离子键。
B.离子键没有饱和性、方向性,因此任何离子周围可以吸引数目不定的异号离子。
C.化学键是相邻粒子间的相互作用力。
D.离子晶体的配位数与配合物的配位数的定义相同
第5题
下列描述配合物的配位数与空间构型关系的说法,正确的是()。
A.中心离子的配位数为2的配合物均为直线型
B.中心离子的配位数为4的配合物均为平面四方形
C.中心离子的配位数为4的配合物均为四面体
D.中心离子的配位数为6的配合物均为立方体
第6题
胆矾化学式
(1)写出下列物质的名称或化学式
|
第8题
根据晶体场理论,下列叙述错误的是()
A.强场配体造成的分裂能较小
B.中心离子的d轨道在晶体场的作用下分裂
C.配离子的颜色和d电子吸收一定波长的光有关
D.通常在弱场配体作用下,容易形成高自旋的配合物
第9题
第一电离能的变化规律
| [化学—物质结构与性质] (1)依据第2周期元素第一电离能的变化规律,参照下图B、F元素的位置,用小黑点标出C、N、O三种元素的相对位置。
(2)NF3可由NH3和F2在Cu催化剂存在下反应直接得到:4NH3+3F2 ①上述化学方程式中的5种物质所属的晶体类型有_________(填序号)。 a.离子晶体 b.分子晶体 c.原子晶体 d.金属晶体 ②基态铜原子的核外电子排布式为________。 (3)BF3与一定量水形成(H2O)2·BF3晶体Q,Q在一定条件下可转化为R:
①晶体Q中各种微粒间的作用力不涉及___________(填序号)。 a.离子键 b.共价键 c.配位键 d.金属键 e.氢键 f.范德华力 ②R中阳离子的空间构型为_______,阴离子的中心原子轨道采用_______杂化。 (4)已知苯酚( |


 如果结果不匹配,请
如果结果不匹配,请 
依据第2周期元素第一电离能的变化规律,参照下图B、F元素的位置,用小黑](https://img2.soutiyun.com/ask/uploadfile/8826001-8829000/5be2c7272651adbf6344236672ae1f2f.jpg)
依据第2周期元素第一电离能的变化规律,参照下图B、F元素的位置,用小黑](https://img2.soutiyun.com/ask/uploadfile/8826001-8829000/425e0fb021ade3acce0a110821379fea.png) NF3+3NH4F
NF3+3NH4F依据第2周期元素第一电离能的变化规律,参照下图B、F元素的位置,用小黑](https://img2.soutiyun.com/ask/uploadfile/8826001-8829000/6b41e97d0c9ea75e505fefd44eef4754.png)
依据第2周期元素第一电离能的变化规律,参照下图B、F元素的位置,用小黑](https://img2.soutiyun.com/ask/uploadfile/8826001-8829000/0b8da5c6988797c7128e142233bfe8d3.jpg) )具有弱酸性,其Ka=1.1 ×10-10;水杨酸第一级电离形成的离子
)具有弱酸性,其Ka=1.1 ×10-10;水杨酸第一级电离形成的离子依据第2周期元素第一电离能的变化规律,参照下图B、F元素的位置,用小黑](https://img2.soutiyun.com/ask/uploadfile/8826001-8829000/8c83ad0997bd73e4e61b8de014677ec5.jpg) 能形成分子内氢键。据此判断,相同温度下电离平衡常数Ka2(水杨酸)_______Ka(苯酚)(填“>”或“<”),其原因是__________。
能形成分子内氢键。据此判断,相同温度下电离平衡常数Ka2(水杨酸)_______Ka(苯酚)(填“>”或“<”),其原因是__________。