 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
短周期主族元素 X 、 Y 、 Z 、 W 的原子序数依次增大。 X 原子的最外层电子数是其内层电子数的 2 倍 ,Y 是地壳中含量最高的元素 ,Z 2+ 与 Y 2- 具有相同的电子层结构 ,W 与 X 同主族。下列说法中正确的是()
A.原子半径的大小顺序 :W>Z>Y>X
B.Y 与 X 只能形成一种化合物
C.X 的最高价氧化物对应水化物的酸性比 W 的弱
D.Y 的气态简单氢化物的热稳定性比 W 的强
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.原子半径的大小顺序 :W>Z>Y>X
B.Y 与 X 只能形成一种化合物
C.X 的最高价氧化物对应水化物的酸性比 W 的弱
D.Y 的气态简单氢化物的热稳定性比 W 的强
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“短周期主族元素 X 、 Y 、 Z 、 W 的原子序数依次增…”相关的问题
更多“短周期主族元素 X 、 Y 、 Z 、 W 的原子序数依次增…”相关的问题
A.原子最外层电子数由多到少的顺序:Y、X、W、Z
B.原子半径由大到小的顺序:W、Z、Y、X
C.元素非金属性由强到弱的顺序:Z、W、X
D.简单气态氢化物的稳定性由强到弱的顺序:X、Y、W
(1)W位于元素周期表第____周期第____族,其基态原子最外层有____个电子。
(2)X的第一电离能比Y的____(填“大”或“小”),1mol X22-中含有的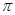 键数目为____。
键数目为____。
(3)X和Y的气态氢化物中,较稳定的是____(写化学式),Y的同族元素(包括Y)的最简单氢化物中沸点最低的是____。
(4)写出KZY3与HZ浓溶液反应制取Z2的化学方程式,并标出电子转移的方向和数目____。
(5)已知:X(s)+Y2(g)=XY2(g) ΔH1= -393.5 kJ?mol-1
XY(g) +1/2Y2(g)=XY2(g) ΔH2= -282.9 kJ?mol-1
则X(s)与Y2(g)反应生成XY(g)的热化学反应方程式为____。
A.原子半径:丁>丙>乙>甲
B.单质的氧化性:乙>丙>丁
C.气态氢化物稳定性:乙>丙>丁
D.甲与乙、丙、丁形成的化合物均为共价化合物
A.外层电子排布为3d54s1
B.该元素为第四周期、VIB族元素铬
C.+3价离子的外层电子排布式为3d24s1
D.该元素的最高价氧化物的水合物为强酸
A.粒子半径大小关系是X n- >Y n+
B.Z一定是稀有气体元素
C.原子序数关系是Z>Y>X
D.原子半径关系是X<Z<Y