 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
某种氢氧燃料电池的电解液为 KOH 溶液,下列有关该电池的叙述不正确的是( )。
A.用该电池电解 CuCl2溶液,产生2.24L Cl2(标准状况)时,有0.1mol 电子转移
B.工作一段时间后,电解液中 KOH 的物质的量不变
C.该燃料电池的总反应方程式为:2H2+O2=2H2O
D.正极反应式为:O2+2H2O+4e-=4OH
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.用该电池电解 CuCl2溶液,产生2.24L Cl2(标准状况)时,有0.1mol 电子转移
B.工作一段时间后,电解液中 KOH 的物质的量不变
C.该燃料电池的总反应方程式为:2H2+O2=2H2O
D.正极反应式为:O2+2H2O+4e-=4OH
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“某种氢氧燃料电池的电解液为 KOH 溶液,下列有关该电池的叙…”相关的问题
更多“某种氢氧燃料电池的电解液为 KOH 溶液,下列有关该电池的叙…”相关的问题
A.负极反应式为:CH4+10OH--8e=CO32-+7H2O
B.负极反应式为:O2+2H2O+4e=4OH
C.随着放电的进行,溶液的 pH 不变
D.放电时溶液中的阴离子向正极移动
50ml、0.1mol/L的某一元己弱酸HA溶液与20ml、0.10mol/L的KOH溶液混合,并加水稀释至100ml,测得该溶液的pH=5.25。此一元弱酸的电离常数为()。
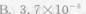
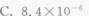
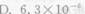
A.Cu<5
B.Cu≥5
C.Cu 10
D.5< Cu <10
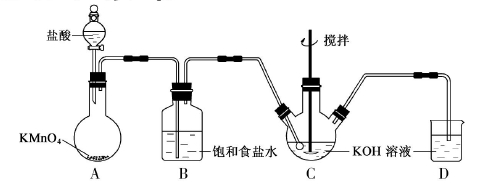
(1)装置A中KMnO4与盐酸反应生成MnCl2和Cl2,其离子方程式为_____________(填化学式)。
(2)Cl2和KOH在较高温度下反应生成KClO3在不改变KOH溶液的浓度和体积的条件下,控制反应在0℃~5℃进行,实验中可采取的措施是_________。
(3)制备K2FeO4时,KClO饱和溶液与Fe(NO3)3饱和溶液的混合方式为_______。
(4)提纯K2FeO4粗产品[含有Fe(OH03、KCl等杂质]的实验方案为:将一定量的K2FeO4粗产品溶于冷的3mol·L-1KOH溶液中,_____(实验中须使用的试剂有:饱和KOH溶液,乙醇;除常用仪器外须使用的仪器有:砂芯漏斗,真空干燥箱)。
某种溶液的浓度为20%,加入水后溶液的浓度变为15%。如果再加入同样多的水,则溶液浓度变为()。
A. 13%
B. 12.5%
C. 12%
D. 10%
垂熔玻璃滤器使用后用水抽洗,并以某种溶液浸泡处理,该溶液为
A.重铬酸钾一浓硫酸液
B.硝酸钠一浓硫酸液
C.浓硫酸液
D.亚硝酸钠一浓硫酸液
E.30%H202